Belangrijk verschil: de rangschikking van atomen in een molecuul helpt de polariteit ervan te bepalen. Een molecuul is polair, als het een positieve en een negatieve lading heeft. Een niet-polair molecuul is een molecuul met minder lading.
In de chemie verwijst polariteit naar de scheiding tussen elektrische ladingen van een molecuul of zijn chemische groep met een elektrisch dipool- of meerpoolmoment. Polaire moleculen interageren door intermoleculaire bindingen en waterstofbruggen. Moleculaire polariteit is afhankelijk van het verschil in elektronegativiteit tussen atomen in een molecuul. Polariteit, bepaalt ook een aantal fysieke eigenschappen zoals oppervlaktespanning, smelt- en kookpunten en oplosbaarheid.
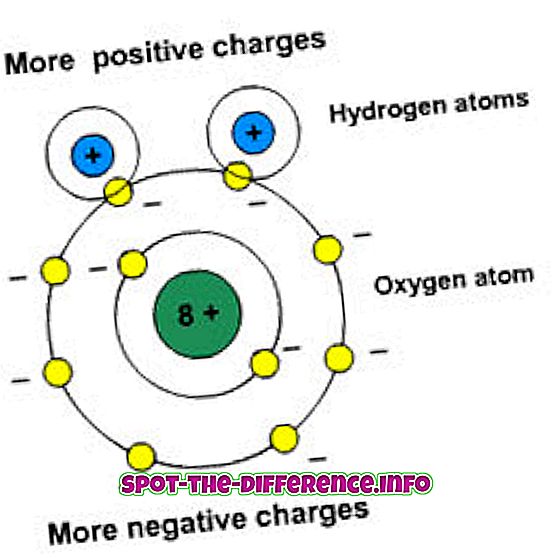
Polariteit betekent de scheiding van de ladingen. Deze moleculen hebben een dipoolmoment. Het Dipool-moment meet de polariteit van een binding. Polaire stoffen hebben een wisselwerking met andere polaire elementen.

Een niet-polair molecuul heeft niet genoeg lading. Niet-polaire moleculen worden op een manier van symmetrie verdeeld en hebben geen groot aantal elektrische ladingen erop. Wanneer twee atomen of twee dezelfde atomen dezelfde elektronbinding tussen hen hebben, trekken de atomen aan het elektronenpaar. Deze aantrekkingskracht helpt hen om elektronen te delen en dit soort delen van bindingen tussen moleculen staat bekend als niet-polaire covalente bindingen.
Vergelijking tussen Polar en niet-Polar:
Polair | Non-Polar | |
Definitie | Polaire stoffen hebben een positieve en een negatieve lading op het atoom. | Niet-polaire substanties hebben geen grote ladingen op het verbonden atoom. |
Beweging | Ze hebben een elektrische dipoolbeweging. | Ze hebben geen dipoolbeweging. |
Lading scheiding | Er is ladingsscheiding. | Er is geen ladingsscheiding. |
wisselwerking | Ze werken samen met andere polaire stoffen. | Ze hebben geen wisselwerking met andere polaire stoffen. |
Voorbeeld | Water, alcohol en zwavel. | Olie. |