Belangrijk verschil: Atomen zijn de basiseenheden waarvan alle materie is gemaakt. Atomen van verschillende elementen komen samen om moleculen te maken. Dit gebeurt via een chemische reactie. Een molecuul is de kleinste hoeveelheid van een chemische stof die kan bestaan. In wezen is een verbinding een type molecuul. Een molecuul kan bestaan uit twee of meer atomen van hetzelfde element of twee of meer atomen van verschillende elementen. Verbindingen zijn echter moleculen die bestaan uit atomen van verschillende moleculen.
Een element is een zuivere chemische substantie die een of een type atoom heeft, onderscheiden door zijn atoomnummer. Het atoomnummer is afgeleid van het aantal protonen dat aanwezig is in de kern van het element. Er zijn in totaal 118 elementen geïdentificeerd, verdeeld over metaal, metalloïden en niet-metalen. Elk element heeft zijn eigen set eigenschappen. De meeste elementen zijn beschikbaar op de aarde, terwijl een paar kunstmatig zijn ontwikkeld door kernreacties. Een element is al in zijn ruwste vorm en kan niet verder worden afgebroken. Alle elementen zijn te vinden in het periodiek systeem, opgesomd met atoomnummer.
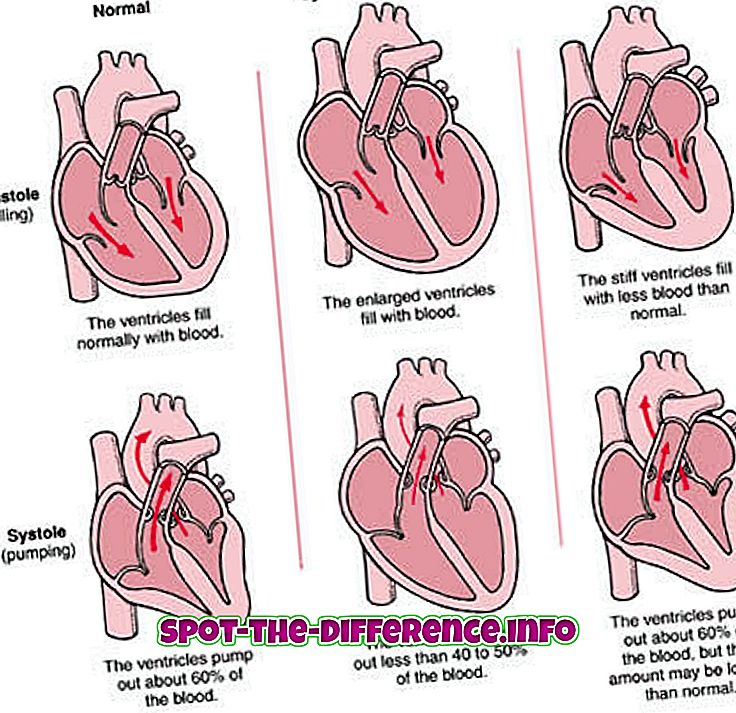
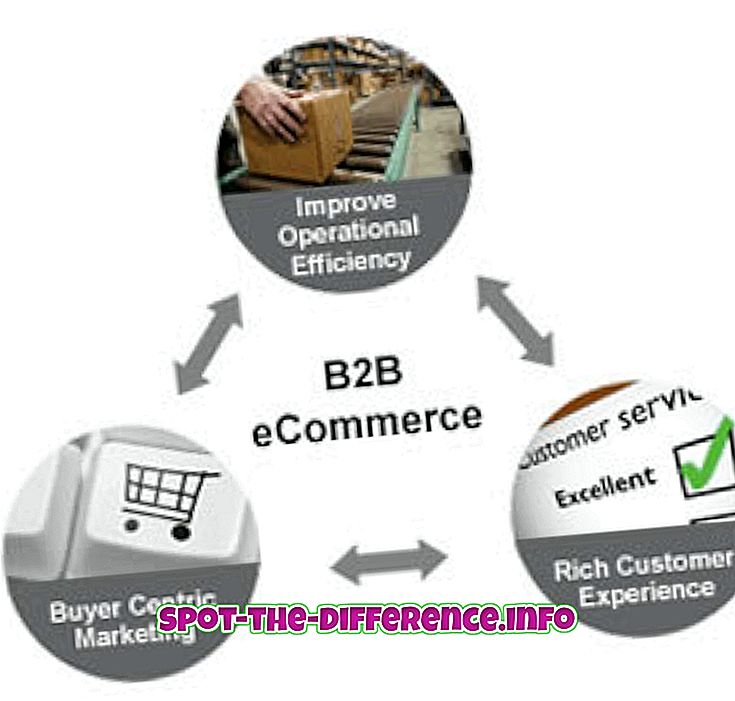
Atomen van verschillende elementen komen samen om moleculen te maken. Dit gebeurt via een chemische reactie. Bijvoorbeeld: twee waterstofatomen en één zuurstofatoom worden gecombineerd om een watermolecuul te maken.
Een molecuul is de kleinste hoeveelheid van een chemische stof die kan bestaan. Zoals de kleinste hoeveelheid water die men kan hebben, is een molecuul water of H20. Het is gemaakt van verschillende atomen samen; vandaar dat het terug kan worden gescheiden in de verschillende atomen.
Een molecuul kan heel andere eigenschappen hebben dan de elementen waaruit het is gemaakt. Bijvoorbeeld: water gedraagt zich heel anders dan zuurstof of waterstof, hoewel het bestaat uit twee waterstofatomen en één zuurstofatoom.
Bovendien kan een atoom niet onafhankelijk in de natuur bestaan zonder ergens aan te hechten. We zullen nooit slechts een enkel zuurstofatoom of een enkel koolstofatoom vinden. Het is altijd verbonden met iets, zoals O2 (zuurstof) of CO2 (koolstofdioxide). Wanneer het molecuul in een molecuul is gebonden, kan het onafhankelijk in de natuur bestaan. Daarom kunnen we altijd een molecuul zuurstof, een molecuul koolstofdioxide, een molecuul water (H2O), enz. Vinden.

Moleculen hebben de neiging om te groeperen, hun vorming is afhankelijk van hun toestand. Zoals in een gasvormige toestand neigen de moleculen er gewoon rond te vliegen. In vloeibare toestand hebben de moleculen de neiging om losjes bij elkaar te worden gegroepeerd, zodat ze nog steeds kunnen bewegen. Terwijl in vaste toestand de moleculen dicht op elkaar gepakt zijn en alleen kunnen trillen.
Moleculen worden meestal weergegeven in een molecuulformule. Bijvoorbeeld: O2, H2O, CO2, C6H12O6 (suiker). De molecuulformule is de naam van het element gevolgd door het aantal atomen van dat element in het molecuul.
In wezen is een verbinding een type molecuul. Een molecuul kan bestaan uit twee of meer atomen van hetzelfde element of twee of meer atomen van verschillende elementen. Verbindingen zijn echter moleculen die bestaan uit atomen van verschillende elementen. Daarom kan worden gezegd dat alle verbindingen moleculen zijn, maar niet alle moleculen zijn verbindingen.
Dus, waterstof (H2), zuurstof (O2), stikstof (N2), water (H2O), koolstofdioxide (CO2) en methaan (CH4) zijn allemaal moleculen. Alleen Water (H2O), koolstofdioxide (CO2) en methaan (CH4) zijn echter verbindingen, de andere niet.