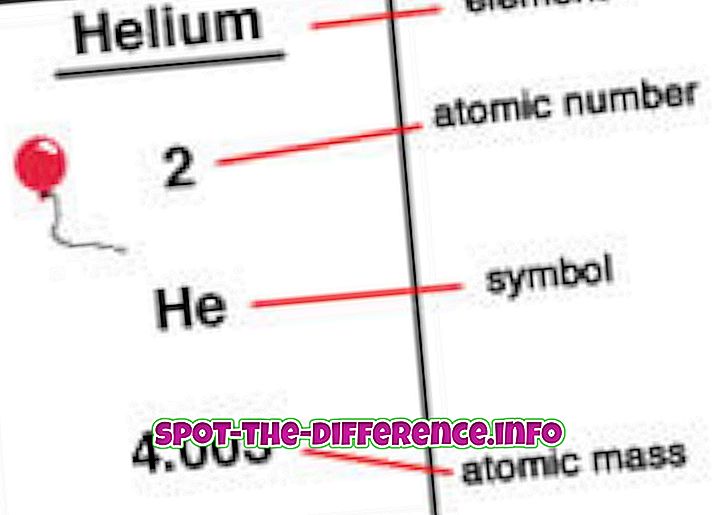
Belangrijkste verschil: Atomaire massa is eenvoudigweg de massa van een specifieke isotoop, of de gecombineerde massa van de protonen, neutronen en elektronen van het atoom. Atoomnummer is het aantal protonen dat wordt gevonden in een kern van een element.
Laten we eerlijk zijn chemie is verwarrend, de verschillende hoeveelheid elementen, atoomnummers, bindingen, massa, gewicht, atomen, etc. Al deze woorden beginnen te vervagen na een bepaalde tijd dat een persoon niet langer de een van de ander kan onderscheiden. Goed atomaire massa en atoomnummer zijn twee van dergelijke woorden die vaak verward en door elkaar gebruikt worden.
De atoommassa is de massa van een atoom wanneer het in rust is. Dit komt omdat wanneer een atoom met een zeer hoge snelheid beweegt, het de neiging heeft in massa toe te nemen. Hoewel volgens de definitie de atoommassa de massa van alle protonen, neutronen en elektronen is, zijn elektronen te klein om een significant verschil in de atomaire massa te maken. De meeste elementen op het periodiek systeem hebben isotopen en vanwege het verschil in de neutronentelling verandert ook de massa van elk isotoop.
De atomaire massa wordt uitgedrukt met atomaire massa-eenheden of amu. Eén atomaire massa-eenheid is gelijk aan 1/12 van de massa van koolstof-12. Wanneer de massa van een atoom wordt gedeeld door de 1 / 12e van de massa van koolstof-12, wordt de relatieve massa van het element verkregen. Relatieve massa van een object is echter feitelijk het atoomgewicht van een element, zoals berekend door alle isotopen te beschouwen. Dit mag echter niet worden aangenomen als atomaire massa van een element.

Atoomnummer is het aantal protonen dat wordt gevonden in een kern van een element. Wanneer een atoom neutraal is, betekent dit dat het hetzelfde aantal protonen en elektronen heeft. Atoomnummer wordt aangegeven met een Z. Omdat elk element een ander aantal protonen heeft, wordt dit getal ook gebruikt om een element weer te geven. Isotopen delen gewoonlijk hetzelfde atoomnummer maar worden geclassificeerd met hun atoommassa, bijvoorbeeld koolstof-12, koolstof-13.
Elementen worden op volgorde van atoomnummer op een periodiek systeem geplaatst. Het atoomnummer staat in de linkerbovenhoek van het element als een superscript. Atoomnummers kunnen helpen informatie over het element te onthullen en veel mensen kunnen het atoomnummer zien en aangeven welk element het is. Het geeft ook aan waar het in het periodiek systeem kan worden geplaatst en of het vloeibaar, gasvormig of vast is. Atoomnummer geeft ook informatie over kernlading, oxidatietoestanden, verbindingsgedrag, lading van het ion, etc.






























