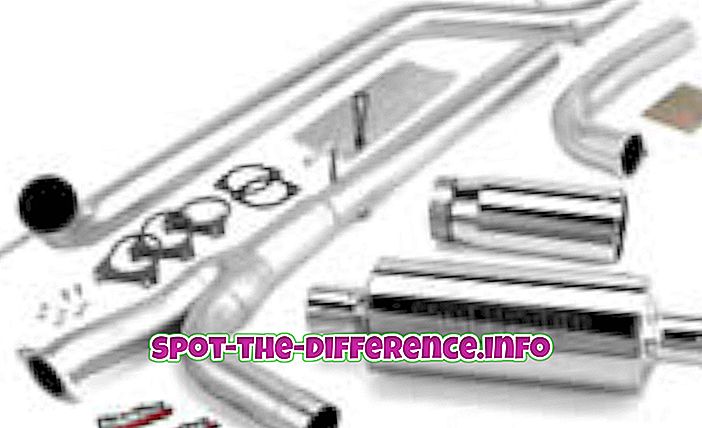
Belangrijkste verschil: Absorptie is een bulkverschijnsel waarbij een absorbeermiddel volledig doordringt in het lichaam van een vaste stof of vloeistof om een verbinding of een oplossing te vormen. Aan de andere kant is adsorptie een oppervlakteverschijnsel waarbij moleculen van een adsorbaat zich alleen concentreren op het oppervlak van een adsorbens.
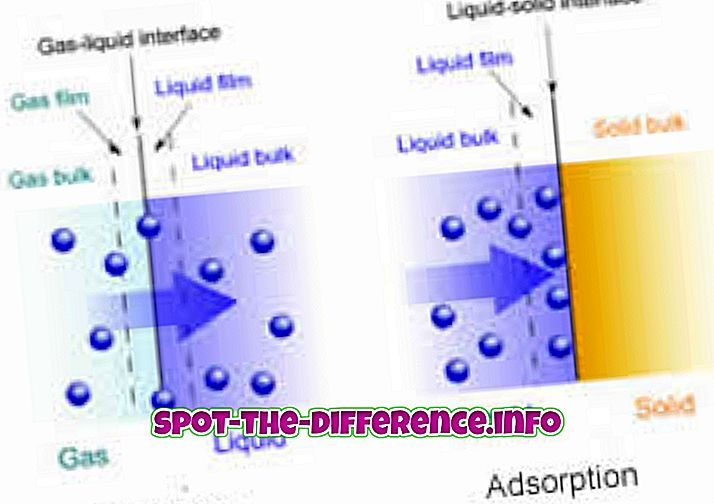
Chemische reactie - kooldioxide geabsorbeerd door een oplossing van kaliumkoolstof
Fysisch proces - Lucht geabsorbeerd in water door op te lossen

Er zijn twee soorten adsorptiemodi: chemisch en fysiek. Bij chemische adsorptie zijn de moleculen en het oppervlak gebonden door zwakke Vander Walls-krachten. Aan de andere kant wordt bij chemische adsorptie een chemische binding gevormd tussen moleculen en het oppervlak.
Daarom is het belangrijkste verschil tussen adsorptie en absorptie dat absorptie een bulkverschijnsel is, wat betekent dat dit door het hele lichaam van het materiaal gebeurt, terwijl adsorptie nog steeds een oppervlakteverschijnsel is. Adsorptie is altijd exotherm, terwijl absorptie endotherm is. Sorptie omvat beide processen van absorptie en adsorptie.
Vergelijking tussen adsorptie en absorptie:
adsorptie | Absorptie | |
definitie | Ophoping van een gas of vloeibare opgeloste stof op het oppervlak van een vaste stof of een vloeistof | Diffusie van een stof in een vloeistof of vaste stof om een oplossing of verbinding te vormen |
Voorbeeld | Inerte gassen worden geadsorbeerd op houtskool. | Een droge spons absorbeert water |
Warmte uitwisseling | Exotherm met uitzondering van adsorptie van H2 op glas | endotherme |
Evenwicht bereiken | Relatief sneller | Relatief langzaam |
Concentratie | De concentratie op het oppervlak van het adsorbens is anders dan in de bulk | Concentratie blijft hetzelfde in het hele materiaal |
Snelheid van voorkomen | Het is aanvankelijk snel maar later begint het tempo te dalen | Het gebeurt op uniforme snelheid |